La tuberculose bovine - Un défi sanitaire, économique et éthique
Hélène Soubelet
Vétérinaire, directrice générale de la Fondation pour la recherche sur la biodiversité (FRB).
Petite histoire évolutive du complexe Mycobacterium tuberculosis1
Ce complexe, probablement originaire d'Afrique de l'Est, a co-évolué avec l'humain depuis 70 000 ans. Il est constitué de plusieurs espèces présentant plus de 99 % de similarité génétique, certaines de ces lignées spécialisées dans les humains (M. tuberculosis, M canetii et M africanum) et d'autres dans les animaux (M . bovis, M caprae, M pinipedi et M microti). Les espèces pathogènes pour les animaux auraient émergé à partir de M. africanum, au Néolithique, il y a environ 10 000 ans.
Une transmission plus complexe qu'il n'y paraît
La transmission de la bactérie, chez l'homme comme chez les bovins, se produit principalement par inhalation d'aérosols contaminés à partir d'individus infectés et à la faveur de contacts étroits au sein de l'espèce. Plus il y a concentration d'individus, plus la bactérie se propage rapidement. Chez les humains, la maladie est restée sporadique jusque dans les années 1700 avant de devenir épidémique à la faveur de la révolution industrielle.1 Chez les animaux, elle a été favorisée par l'augmentation de la taille des cheptels et surtout par l'augmentation des échanges de bovins.
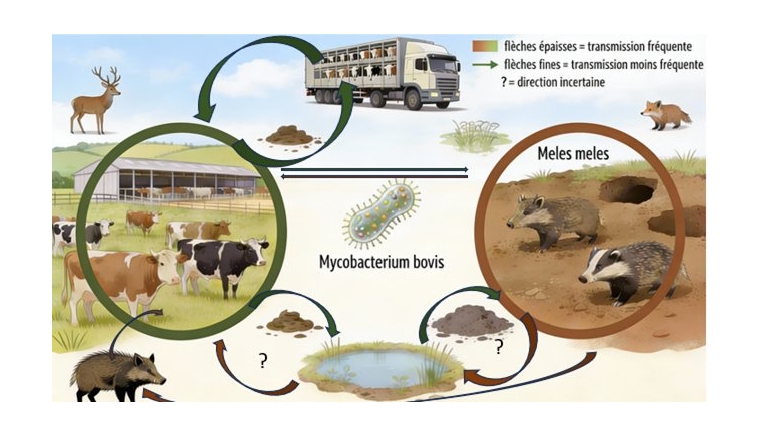
En France, la contamination de la faune sauvage s'est effectuée à partir des bovins ; pendant longtemps, la recontamination à partir de la faune sauvage est restée hypothétique. Depuis, plusieurs travaux de surveillance ont mis en évidence la circulation de Mycobacterium bovis dans certaines populations sauvages (notamment cervidés et blaireaux) avec des souches identiques à celles des cheptels voisins, suggérant la constitution possible de réservoirs environnementaux et un risque de transmissions « retour » vers les bovins. Dans toutes les espèces sensibles, M. bovis peut être excrété dans le mucus oro-nasal, les expectorations, l'urine, les fèces et les sécrétions de plaies. Une circulation triangulaire, identifiée par les analyses phylogénomiques menées entre 2010 et 2017 en Côte-d'Or et Nouvelle-Aquitaine, suggère que les sangliers pourraient jouer un rôle d'hôte intermédiaire dans la persistance et la circulation des souches de Mycobacterium bovis dans ces régions endémiques françaises.2
La bactérie s'inscrit dans ce qu'on appelle un système multi-hôtes qui rend son éradication difficile, en raison des réservoirs sauvages (cervidés, sangliers, blaireaux) et domestiques (bovins, canins, porcins) qui se contaminent mutuellement et contaminent leur environnement (Figure 1).
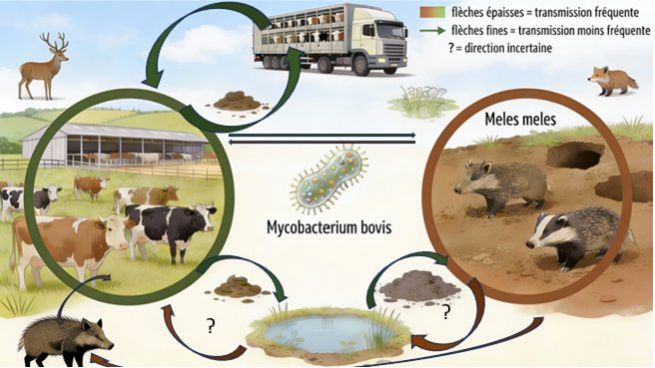
Une survie dans l'environnement qui pose problème
Les connaissances récentes montrent que le complexe M. bovis n'est pas strictement intracellulaire et qu'il est capable de survivre, voire de se multiplier, dans l'environnement. Plusieurs études expérimentales ont montré que la bactérie pouvait rester infectieuse dans les agrosystèmes pendant des semaines, voire des mois. La transmission est donc également indirecte par le sol, les pâtures, les points d'eau. Elle contamine aussi les fumiers et lisiers pendant environ 6 mois.
Des facteurs climatiques semblent également jouer un rôle important. La bactérie résiste mieux et plus longtemps dans les fèces, les aliments, l'eau et le sol dans des conditions froides, humides et peu soumises au rayonnement solaire ultraviolet.
Seul un stockage très long ou un compostage à plus de 50°C réduit significativement ou élimine les risques. Or, désinfecter l'environnement n'est évidemment pas possible, ce qui pose la question de la durée de sa survie. Là encore, la réponse n'est pas simple.
Barbier et al.3 ont montré que des sols contaminés se négativaient après 60-120 jours à 22°C, alors qu'à 4 °C la bactérie était encore détectable après 150 jours.
Par des études expérimentales, Fine et al.4 ont montré une persistance de M. bovis dans l'environnement, significativement plus courte au printemps et en été (1 à 2 mois contre 6 mois en automne et hiver) en raison des températures moyennes journalières les plus élevées. Ils démontrent la persistance de M. bovis jusqu'à 88 jours dans le sol, 58 jours dans l'eau et le foin, et 43 jours dans le maïs.
Ces études illustrent que les bactéries M. bovis persistent suffisamment longtemps pour représenter un risque d'exposition pour les bovins et la faune sauvage.
L'intégration des dimensions écologiques (faune réservoir, environnement contaminé, conditions climatiques) est indispensable pour mieux comprendre les modèles de transmission et adapter les stratégies de gestion.
En résumé :
- La transmission intra espèce domine,
- Pour les bovins, les échanges entre cheptels sont les facteurs de risques principaux,
- Les contacts directs entre les blaireaux et les bovins sont rares,
- La contamination environnementale joue un rôle crucial et pourrait expliquer certaines réinfections après abattage total.
Abattage des blaireaux, entre controverses scientifiques et effets paradoxaux
Depuis que le blaireau a été identifié comme réservoir sauvage de la maladie dans les années 1970, il a également été vu par certains comme une explication à la crise et une voix de sortie toute trouvée pour l'action publique, plus simple à gérer qu'une réforme du modèle agricole ou des règles sanitaires sur les échanges d'animaux. La mise en évidence d'un réservoir sauvage complique considérablement les efforts d'éradication dans les troupeaux bovins, mais le point crucial est de s'assurer qu'il joue un rôle déterminant dans la diffusion de la maladie et que les mesures de gestion de ce réservoir sont efficaces.5
Pour le savoir, des essais randomisés d'abattages massifs ont été menés en Angleterre entre 1998 et 2005, comparant l'incidence de la tuberculose bovine dans 10 zones témoins (sans intervention) à 10 zones soumises à deux stratégies d'abattage. Une publication scientifique de 20066 a documenté une diminution de l'incidence de la tuberculose dans les zones d'abattage et une augmentation paradoxale de la tuberculose en dehors de ces zones.
Fortes des résultats de cet essai randomisé, les autorités ont mis en place en 2013 un grand plan d'abattage dont l'intensité a généré une importante controverse scientifique, entre interprétation, réinterprétation et contestations réciproques.7
Les débats ont été particulièrement vifs après que plusieurs études8,9, réexaminant les données de 2006, ont conclu que l'analyse statistique était fausse et qu'une fois corrigée, cet essai ne mettait en évidence aucun effet positif de l'abattage, ni même d'effet de perturbation. Le ministère de l'environnement, de l'alimentation et des affaires rurales du Royaume Uni a finalement reconnu en 202510 que si les mesures mises en oeuvre avaient permis de réduire les foyers de tuberculose, il n'était pas statistiquement possible de dissocier les effets de l'abattage des autres mesures introduites simultanément (en particulier, l'utilisation systématique du test de dépistage de l'interféron gamma) et que les preuves d'un effet positif de l'abattage des blaireaux n'étaient pas aussi solides que le suggéraient les analyses initiales.
Par ailleurs, une étude menée par l'institut de zoologie de Londres et l'Université d'Oxford11 a démontré que l'abattage massif ou systématique dans les populations de blaireaux pouvait engendrer des effets secondaires contre-productifs avec perturbation du comportement des animaux survivants :
- Dispersion accrue des individus survivants vers des zones nouvelles,
- Augmentation des contacts interspécifiques potentiels,
- Perturbation de la structure sociale pouvant favoriser la transmission intraspécifique,
- Augmentation de 61 % de la taille des domaines vitaux mensuels des blaireaux survivants,
- Augmentation de 39 % de la distance maximale parcourue chaque nuit,
- Visites de 45 % de champs supplémentaires chaque mois, augmentant ainsi les opportunités de contact avec le bétail.
Ces éléments combinés plaident pour une approche plus éthique dans la gestion de la maladie. Paul Torgerson, professeur d'épidémiologie vétérinaire à l'université de Zurich conclut dans son article résumant la situation fin 20259 que, « si les analyses avaient été correctement effectuées en 2006, il n'y aurait sans doute pas eu d'abattage massif de blaireaux en 2013, ce qui aurait eu pour conséquences positives une économie substantielle d'argent, une conduite plus éthique vis-à vis de la faune sauvage et une recherche plus efficace des véritables causes de l'épidémie de tuberculose bovine ». Il recommande que les articles scientifiques qui s'appuient sur les analyses erronées de la campagne d'abattage conduite entre 1998 et 2005 soient corrigés ou rétractés et que l'abattage massif de blaireaux soit retiré des « outils » pour lutter contre la tuberculose.
Alors, on vaccine ?
En 2013, alors que l'Angleterre lançait son programme d'abattage industriel des blaireaux, le Pays de Galles a opté pour une politique de vaccination.
La vaccination contre la tuberculose est relativement efficace pour faire baisser la pathogénicité de la maladie et en diminuer la circulation. Cependant, en l'absence de test fiable pour discriminer les animaux vaccinés des animaux contaminés, la vaccination est interdite pour les bovins en Europe.
Les données scientifiques publiées à ce jour indiquent que la vaccination des blaireaux peut contribuer à la maîtrise de la prévalence de la tuberculose bovine chez les blaireaux sauvages et gagnerait à être intégrée à une stratégie plus globale de lutte contre cette maladie.12 La vaccination présente au moins trois avantages par rapport à l'abattage :
- Elle permet une réduction de la prévalence de la tuberculose chez les blaireaux vaccinés,
- Elle n'engendre pas de perturbations comportementales responsables des effets paradoxaux de diffusion de la tuberculose,
- Elle a la faveur du grand public car c'est une approche plus durable et éthiquement acceptable.
Peut-on envisager un nouveau protocole de gestion ?
Le protocole de gestion en France est basé sur la tuberculination et l'abattage total ou partiel sous conditions13, dans le cadre d'un plan national d'éradication complété par des mesures de biosécurité en zones à risques. La surveillance est majoritairement basée sur la tuberculination (forte ou comparative) et la recherche d'interféron gamma afin d'identifier précocement les cheptels atteints et conserver le statut indemne permettant les exports (incidence de la maladie inférieure à 0,1 %). Une des difficultés est que la période d'incubation chez les bovins peut atteindre plusieurs mois, voire des années chez les adultes. Plusieurs contrôles couvrant la période d'incubation et la période de positivation des tests sont donc nécessaires pour être certains qu'un troupeau est indemne.
En France, une étude a comparé l'abattage total à six protocoles de dépistage et d'abattage, dont deux versions du protocole officiel et quatre alternatives faisant varier les délais des tests et la nature des tests.14 Trois indicateurs clés ont été calculés pour chaque protocole : son efficacité épidémiologique (probabilité d'échec), son coût global et le taux d'abandon (en pourcentage d'éleveurs qui adoptent finalement l'abattage total). La probabilité d'échec en fonction des protocoles varie de 1,4 % à 12,4 % et est nulle (par définition) pour l'abattage total. Le coût médian varie entre 2 700 € et 78 000 € pour les protocoles de dépistage avec un coût d'abattage total le plus élevé à environ 120 000 €. Le taux d'abandon varie de 7,8 % à 22 %. Les chercheurs concluent que le compromis optimal entre efficacité épidémiologique, coût public et taux d'abandon est obtenu pour les protocoles prévoyant un allongement du délai (6 mois au lieu de 2 dans le protocole officiel) entre les deux dernières séances de dépistage, avec 2 ou 3 séances au total. Ils concluent également que l'utilisation de trois indicateurs d'efficacité (au lieu d'un seul : l'efficacité épidémiologique), pourrait contribuer à améliorer le protocole officiel de dépistage et d'élimination appliqué en France en mettant en oeuvre des protocoles alternatifs, très efficaces, moins coûteux et mieux acceptés que l'abattage total.
Conclusion
Plus largement, la gestion de ces maladies infectieuses à incidences économiques doit être questionnée éthiquement, car les mesures de gestion comme l'abattage peuvent conduire à des difficultés économiques et sociales pour les éleveurs touchés15, des diminutions du bien-être animal, des questionnements éthiques relatifs à l'élimination d'espèces sauvages et à l'équité dans la contribution au maintien du statut indemne. Si ceux qui subissent les mesures de gestion sont également ceux qui bénéficient du statut indemne, l'équation est simple. Malheureusement, ce n'est pas toujours le cas. Par exemple, les mesures d'abattage total peuvent mettre en difficulté des filières locales n'exportant pas d'animaux vivants. Ces filières payeront donc le prix du maintien du droit à exporter pour d'autres productions. Dans un contexte économique contraint et verrouillé, ce débat sur les dimensions sociales et éthiques est difficile, mais il est indispensable. Pour une meilleure adhésion aux mesures de gestion, celles-ci doivent être co-construites, fondée sur la confiance ; les actions doivent rester proportionnées, et les coûts supportés par certains éleveurs pour le bénéfice collectif doivent être transparents et reconnus.16,17
Références bibliographiques :
1. Paupy, C., Blanc, S., Boëtsch, G., Hossaert-Mckey, M., Renaud, F., Thiébault, S. et al. (2017). Écologie de la santé : pour une nouvelle lecture de nos maux.
2. Canini, L., Modenesi, G., Courcoul, A., Boschiroli, M. L., Durand, B., Michelet, L. (2023). Deciphering the role of host species for two Mycobacterium bovis genotypes from the European 3 clonal complex circulation within a cattle-badger-wild boar multihost system. MicrobiologyOpen, 12(1), e1331.
3. Barbier, E., Rochelet, M., Gal, L., Boschiroli, M. L., Hartmann, A. (2017). Impact of temperature and soil type on Mycobacterium bovis survival in the environment. PloS one, 12(4), e0176315.
4. Fine, A. E., Bolin, C. A., Gardiner, J. C., Kaneene, J. B. (2011). A study of the persistence of Mycobacterium bovis in the environment under natural weather conditions in Michigan, USA. Veterinary medicine international, 2011(1), 765430.
5. Soubelet, H. (2020). Approche systémique des conséquences (avantages et inconvénients) de l'abattage de la faune sauvage comme méthode de gestion des maladies infectieuses. Fondation pour la recherche sur la biodiversité.
6. Donnelly, C.A., Woodroffe, R., Cox, D.R., et al. Positive and negative effects of widespread badger culling on tuberculosis in cattle. Nature 2006; 439: 843-6
7. Torgerson, P. R., Hartnack, S., Rasmussen, P., Lewis, F. I., O'Donnell, P., Langton, T. E. (2025). Randomised Badger Culling Trial-no effects of widespread badger culling on tuberculosis in cattle: comment on Mills, Woodroffe and Donnelly (2024a, 2024b). Royal Society Open Science, 12(6), 241609.
8. Langton TES, Jones MW, McGill I. Analysis of the impact of badger culling on bovine tuberculosis in cattle in the high-risk area of England, 2009-2020. Vet Rec 2022; 190:e1384
9. Torgerson PR, Hartnack S, Rasmussen P, et al. Absence of effects of widespread badger culling on tuberculosis in cattle. Sci Rep 2024; 14:16326
10. Defra. Bovine tuberculosis Godfray evidence review update. 2025. https://bit.ly/461G5Jr
11. Ham, C., Donnelly, C. A., Astley, K. L., Jackson, S. Y., Woodroffe, R. (2019). Effect of culling on individual badger Meles meles behaviour: potential implications for bovine tuberculosis transmission. Journal of Applied Ecology, 56(11), 2390-2399.
12. Robertson, A., Chambers, M. A., Smith, G. C., Delahay, R. J., Mcdonald, R. A., Brotherton, P. N. (2025). Can badger vaccination contribute to bovine TB control?
A narrative review of the evidence. Preventive Veterinary Medicine, 238, 106464.
13. https://info.agriculture.gouv.fr/boagri/instruction-2023-52
14. Ladreyt, H., Saccareau, M., Courcoul, A., Durand, B. (2018). In silico comparison of test-and-cull protocols for bovine tuberculosis control in France. Frontiers in Veterinary Science, 5, 265.
15. Sébastien Peytavie. Question écrite n° 14042 : Impact de la tuberculose bovine sur la santé des agriculteurs et agricultrices. Assemblée nationale. 2023
16. Enticott, G. (2023). "Good farmers" and "real vets" : social identities, behaviour change and the future of bovine tuberculosis eradication. Irish Veterinary Journal, 76(Suppl 1), 17.
17. Scheitrum, D. P., Schaefer, K. A., Van Winden, S. (2023). Moral hazard in the British bovine tuberculosis control programme. European Review of Agricultural Economics, 50(2), 624-654.